
지난번 글에서 약전에 대한 설명과
제약회사 QC 시험자가 어떤 실험을 하는지에 대해서 정리해보았다.
이번글에서는
1. 제약회사 실무 영어
2. 미국약전 (USP)에 따른 완제품 품질시험
에 대해서 쓰면서 QC 지원자에게 도움될만한 내용을 정리하고자 한다.
1. 제약회사 실무 영어
최근 몇건의 제약회사 지원자들의 자소서를 첨삭을 했고, QC 지원자의 영어 성적, 수준에 대한 질문도 많이 받았다.
개인적으로 생각하기에
외국계 제약회사, 직접적으로 실사 대응하는 사람이 아닌 이상 영어를 유창하게 할 필요는 없다.
개인적으로는 토익 750 정도 이상이면 실무에 큰 문제는 없다고 생각한다.
- 미국약전(USP), 유럽약전(EP) 보고 실험 가능
- 가이드라인 읽고 이해 가능
이면 실무하는데는 문제없다고 생각한다.
기존적인 실무능력+회화
기존적인 실무능력+작문
= 글로벌 실사 대응자 또는 파트너사와 회의/대응 가능자로서 우대
가 가능하다.
하지만 회사 제품의 해외 수출이 달려있는 글로벌 실사나 파트너사를 대응하는 일을 토익 900이라고 맡기진 않는다.
당연히 유학경험 또는 해외대학 출신 사람들에게 맡기게 된다.
따라서 개인적으로는 토익 750정도 이상이면 다 비슷하다고 본다.
2. 미국약전 (USP)에 따라 완제품 시험
예시로서 USP monograph Rosuvastatin tablets을 가져왔다.
물론 회사에서는 최신버전의 USP에 따라 실험하지만,
구글에 'USP 성분명'으로 검색하면 몇몇 성분의 옛날버전을 찾을 수 있다.

1페이지 부터 차근차근 살펴보자.

Definition: 정의
- NLT: not less than (=이상)
- NMT: not more than (=이하)
따라서 rosuvastatin tablet의 정의는
label에 적힌 rosuvastatin 용량의 90~110%로 함유해야 한다.
예시) rosuvastatin 20mg 정제: rosuvastatin을 18~22mg 함유
Identification: 확인시험
이 정제에 포함된 성분이 rosuvastatin이 맞는지 확인하는 시험이다.
방법 A.
함량시험법을 따라서 준비된 sample solution (tablet을 전처리하여 만든 검액)과
standard solution (rosuvastatin 표준품을 전처리하여 만든 검액)을 각각
UV spectrum으로 분석하여 최대흡광도, 최소흡광도를 나타내는 wavelength가 동일한지 확인
방법 B.
함량시험법을 따라서 준비된 sample solution과 standard solution을 HPLC로 분석하여 피크의 retention time (유지시간)이 동일한지 확인

Assay: 함량시험
Protection all solutions ~from light: 광분해되니 차광플라스크 써서 실험필요
Mobile phase: HPLC의 이동상. 중간에 Chromatographic system에 붙어있어야 하는데
가끔 이상한 곳에 붙어있는 경우가 있다.
Diluent: 전처리를 위한 희석액
USP rosuvastatin RS: USP에서 판매하는 rosuvastatin reference standard의 뜻으로,
그냥 rosuvastatin 표준품으로 이해하면 된다.
stock, standard, sample solution: 보통 농도만 알려주지,
몇 mg을 취해서 몇 mL 플라스크를 쓰라고 친절하게 알려주지 않는다.
예를 들어 standard stock solution은 1mg/mL만 맞으면 되니,
10mg을 취해서 10mL플라스크로 만들어도 되고, 20mg을 취해서 20mL플라스크에 만들어도 된다.
10mg을 취할지, 20mg를 취할지는 보통 제품을 허가 받을때 '기준 및 시험법'에 정해져 있고, 허가받은 시험법에 따라 품질관리기록서가 만들어지므로 시험자 개개인이 몇 mg을 취할지 고민할 필요는 없다.
Suitable filter: 보통 pore size가 0.45㎛인 시린지필터를 사용한다. 용매에 녹지않는 물질 (부형제 등)을 걸러주기 위함이다.
Column: L1으로 채워진 컬럼을 쓰라고 한다. 구글에 USP L1으로 검색하면 컬럼 종류가 나온다.
마찬가지로 L2 등 다른 물질표기를 봤을때도 구글 검색하면 컬럼회사에서 잘 설명한 자료가 나온다
System suitability: 시스템적합성
HPLC 등 기기를 분석하면 항상 기기가 적절한지 확인을 하기위해 시스템적합성 분석을 한다.
보통 6번 연속분석하고, tailing factor가 1.8 이하, 각 분석된 면적값의 RSD가 2.0% 이하이면 적합
함량 기준은 90~110%

Dissolution: 용출시험
함량과 마찬가지로 차광시험
Apparatus 2: USP 711 dissolution 항에 따라 패들법 용출시험이다.
기회가 된다면 USP 711도 보면 좋다. 물론 구글 검색하면 PDF파일로 볼수있다.
Time, tolernace: 정제를 넣고 30분 뒤 샘플링해서 분석 및 계산된 용출률이 75% (Q)이면 용출적합이다.
(Q)가붙은 기준은 아래 대한민국 약전의 설명을 참고하자. (우리나라 말이 편하니까)
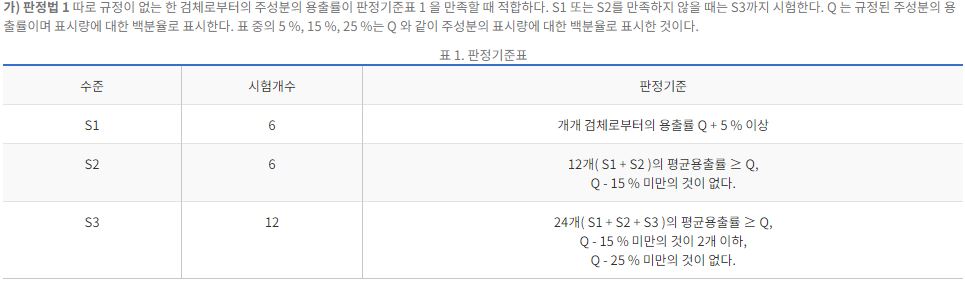

Impurities: 유연물질
함량, 용출과 마찬가지로 차광시험
System suitability: 함량, 용출과는 다르게 시스템적합성 시험이 복잡하다.
유연물질 시험은 rosuvastatin에서 기인한 여러 유연물질의 피크가 겹치지 않고 분리되어야 한다. 따라서 위와 같이 시스템적합성 항목에 resolution (분리도)가 확보되어야 한다.
Relative retention time: 상대적 유지시간. 보통 RRT (알알티)로 부른다.
예를 들어 rosuvastatin의 RT가 10분이라면 related compound A의 RT는 9분이다.
이렇게 RRT를 나타낸 표가 있으면 굳이 related compound A 표준품을 분석해서
RT를 확인해보지 않더라도 해당 위치의 피크가 related compound A임을 알 수 있다.
간단하게 적으려고 했던게 생각보다 적는데 시간이 오래걸렸네요.
도움이 되셨다면 하트 한번씩 눌러주시고
궁금하신게 있으시면 댓글 남겨주세요~
'제약회사 & 바이오' 카테고리의 다른 글
| 제약회사 취업 이직: 제약회사 정보 참고 사이트 TOP 3 (5) | 2023.01.14 |
|---|---|
| 의약품 시장 분석: 아이큐비아(IQVIA), 유비스트(UBIST), 보험청구액(EDI), 영업사원 콜데이터(CSD) 특징 및 장단점 비교 (1) | 2023.01.13 |
| [제약회사 QC] 약전과 품질관리 시험 과정 (0) | 2022.08.03 |
| 제약·바이오 이미지/인포그래픽 그리기 사이트 (0) | 2022.08.03 |
| 제약회사 자기소개서 작성팁 (0) | 2022.08.02 |